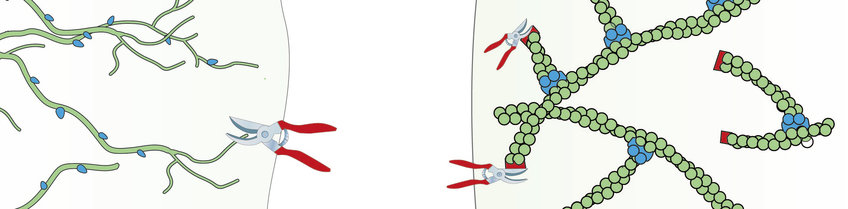
Wie das Stutzen des Zytoskeletts die Zelle bewegt
Interdisziplinäres Team von Max-Planck-WissenschaftlerInnen entschlüsselt rätselhaften Mechanismus der Aktinverzweigung im Zytoskelett
Unsere Zellen zeichnen sich durch Stabilität aus und sind dennoch hoch flexibel. Sie können ihre Form verändern und sich sogar im Gewebe bewegen. Die dafür benötigten Kräfte entstehen durch ein dynamisches Netzwerk aus verzweigten Aktinfilamenten, dem Zytoskelett. Ein interdisziplinäres Team um Peter Bieling und Stefan Raunser vom Max-Planck-Institut für molekulare Physiologie (MPI) in Dortmund hat nun einen bisher unbekannten Mechanismus aufgedeckt, der erklärt, wie das Kappen von alten Aktinfilamenten das Wachstum neuer Filamente fördert. So werden die Struktur und die Funktion des Zytoskeletts aufrechterhalten, genau wie beim Rückschnitt der Hecke im Garten.
Zellen wachsen, teilen sich, verändern ihre Form und bewegen sich. Sie dringen in Wunden ein, um sie zu schließen, oder jagen Bakterien in unserem Blut. Die Beweglichkeit der Zellen ist eine Voraussetzung für eine Vielzahl zentraler biologischer Funktionen und wird durch das Zytoskelett gewährleistet. Dieses dynamisch aufgebaute Proteinnetzwerk setzt sich an der Innenseite der Zellmembran zusammen und verleiht der Zelle ihre Form, ihre mechanische Stabilität und ermöglicht ihre Bewegung.
Wie sich winzige Moleküle zu großen und kraftvollen Strukturen zusammenfügen
Ein wichtiger Bestandteil des Zytoskeletts ist das Protein Aktin, das sich selbst zu langen Filamenten zusammenfügen kann. Aber woher nimmt das Zytoskelett eigentlich die Kraft eine ganze Zelle zu bewegen?
Der Ursprung liegt in einem Keimbildungsprozess, der direkt unter der Zellmembran stattfindet: An die Membran gebundene Nukleationsfaktoren fördern die Bildung eines Aktin-Keims durch den Proteinkomplex Arp2/3. Der Keim, der sich an der Seite eines bestehenden Filaments bildet, entwickelt sich durch die Anlagerung weiterer Aktinmoleküle zu einem neuen Filament, das wie ein Ast aus dem bestehenden Aktinfilament gegen die Zellmembran wächst. So entstehen physikalische Kräfte, die die Membran verschieben können. Die aus dem Keimungsprozess resultierende Struktur des Aktinnetzes erinnert an einen Baum oder eine Hecke mit vielen miteinander verbundenen Ästen aus Aktinfilamenten.
Beschneiden der „Aktin-Hecke“ fördert das Wachstum neuer Filamente
Eine optimale Kraftübertragung auf die Plasmamembran wird durch eine kontinuierliche Pflege des verzweigten Aktin-Netzwerks gewährleistet. Eine wichtige Schlüsselrolle spielt dabei das Capping-Protein, das das Wachstum von Filamenten über eine kritische Länge hinaus verhindert und die Verlängerung von unproduktiven, weit von der Zellmembran entfernten Filamenten stoppt. Das Kappen der Aktinfilamente hat also eine ähnliche Wirkung wie ein pflegender Heckenschnitt: Es hält die (Aktin-)Hecke ordentlich und in Form. Es stimuliert aber auch die Aktinverzweigung (Knospenbildung) in der Nähe der Membran (Pflanzenränder) durch den Arp2/3-Komplex. Wie genau das Capping-Protein die Aktinverzweigung anregt, war bisher nicht bekannt.

Wie ein molekularer Tentakel die Verzweigung antreibt
Dem interdisziplinären Team aus Strukturbiologen und Biochemikern vom MPI in Dortmund, zusammen mit Zellbiologen der Universität Braunschweig, ist es nun gelungen, den bisher rätselhaften Mechanismus hinter der gegenläufigen Funktion des Capping-Proteins aufzuklären. Ein von Felipe Merino, Erstautor der Studie, mittels Kryo-Elektronenmikroskopie erzeugtes hochauflösendes 3D-Bild der Struktur eines Aktinfilaments gebunden an ein Capping-Protein zeigte, dass dieses viel mehr kann als bisher angenommen: Es stoppt nicht nur das Wachstum der Filamente, sondern blockiert über einen tentakelähnlichen Fortsatz die Bindung von keimbildungsfördernden Faktoren. Johanna Funk, ebenfalls Erstautorin der Studie, konnte weiterhin zeigen, dass das Entfernen dieses Tentakels zwar nicht das Kappen der Filamente beeinflusste, aber im Zusammenspiel mit anderen Proteinen des Aktinnetzwerks, dessen Aufbau drastisch hemmte. Dies führte auch zu einer Verringerung der Effizienz von Lamellipodien, die für die Zellbewegung notwendigen armartigen Ausstülpungen.

"Die am Aufbau des Aktinnetzwerks beteiligten Proteine werden häufig als separat voneinander agierende Akteure gesehen. Unsere aus unterschiedlichen Blickwinkeln durchgeführte Untersuchung zur Rolle des Capping-Proteins, hat uns jedoch viel darüber verraten, wie diese Akteure tatsächlich als funktionelle Einheit zusammenarbeiten,“ erklärt Peter Bieling. „Wir hoffen, dass unsere Ergebnisse in Zukunft zu einem besseren Verständnis der Zellbewegung gesunder wie auch kranker Zellen beitragen werden."

